Step 6 of 8
Insuffisance ventriculaire
Une dysfonction ventriculaire est fréquente chez les congénitaux. Elle est liée à plusieurs phénomènes.
- Le remodelage ventriculaire dû à la malformation: insuffisance droite d'un VD sous-aortique fonctionnant comme ventricule systémique, sphérisation d'un ventricule unique (VU), par exemple. La fonction est meilleure lorsque le VU est de type anatomique gauche. La dysfonction diastolique avec baisse de compliance est courante; elle réclame des pressions de remplissage supérieures à la norme.
- La durée de la malformation: plus la correction chirurgicale est tardive, plus le remodelage est important. D’autre part, les opérations palliatives ne protègent pas les ventricules comme le font les corrections totales.
- Le type de surcharge: une surcharge de volume est mieux supportée qu'une surcharge de pression. Cette dernière conduit en effet à une hypertrophie de type concentrique, à une tension de paroi excessive, à une inadéquation du débit coronaire et à une faible tolérance aux déséquilibres du rapport DO2/VO2. Dans un shunt G-D, le VD décompense lorsque la pression systolique pulmonaire augmente au-delà de 50 mmHg ou de 50% de la pression systémique [11]. Une surcharge de volume cause une hypertrophie dilatative, qui peut accommoder une augmentation de volume télédiastolique de l’ordre de 40%. Toutefois, l’efficience de ce ventricule est diminuée, car il travaille sur un grand diamètre (loi de Laplace); il devient très sensible à toute augmentation de postcharge.
- La cyanose: la VO2 myocardique dépasse le DO2 au moindre effort; les épisodes de dysfonction hypoxique sont fréquents. La baisse de la pression de perfusion myocardique due au shunt et les occlusions microvasculaires de l'hyperviscosité induisent une ischémie chronique qui se traduit par des lésions irréversibles (fibrose).
- L'ischémie: elle peut être due à la malformation, à la correction chirurgicale, à la cyanose, aux occlusions microvasculaires de l'hyperviscosité; en cas d’HTAP, elle menace le VD dès que la pression systémique baisse.
Ventricule droit
Chez les congénitaux, l'insuffisance cardiaque concerne le plus souvent le ventricule droit. La surcharge de volume (CIA, insuffisance tricuspidienne ou pulmonaire majeure) entraîne une hypertrophie excentrique et une dilatation du VD; elle est bien tolérée pendant une longue période, mais elle s'accompagne d'un risque élevé d'arythmie ventriculaire réfractaire [3]. Une augmentation chronique de postcharge dès la naissance (sténose pulmonaire, HTAP, VD en position systémique) n’induit pas de dilatation du VD mais une hypertrophie de type concentrique. La fonction droite reste adéquate tant que la pression intraventriculaire est < 50% de la pression gauche et qu’il n’y a pas de surcharge de volume associée (comme lorsque survient une insuffisance tricuspidienne). Les patients deviennent symptomatiques lorsque la pression du VD dépasse la moitié de la pression systémique [11]. Le traitement pharmacologique de l'insuffisance ventriculaire droite est très peu efficace chez les congénitaux (voir Tableau 14.8) [3].
Lorsqu'il est soumis dès la naissance à une postcharge élevée (hypertension pulmonaire, ventricule systémique), le VD conserve sa configuraion fœtale, ne s'amincit pas et reste de la même épaisseur de paroi que le VG; il peut fonctionner ainsi pendant plusieurs décennies. De ce fait, le pronostic de l'hypertension pulmonaire (HTP) congénitale est bien meilleur que celui de l'HTP survenue ultérieurement pendant la vie adulte, puisqu'il est dépendant de la fonction droite [7]. La performance du VD est hautement dépendante de celle du VG, parce que ce dernier contribue pour > 40% à l'éjection droite par la contraction du septum interventriculaire, qui appartient physiologiquement au VG. Cette aide est perdue en cas de large CIV, d'hypoplasie gauche ou de remodelage important des cavités gauches [5]. D'autre part, la dilatation du VD par surcharge de volume comme dans une large CIA repousse le septum à l'intérieur du VG en diastole et restreint le remplissage de celui-ci. S'il s'y ajoute une HTP, la bascule du septum s'installe également en systole; de plus, la durée de l'éjection systolique du VD est prolongée lorsque la postcharge droite est élevée et les pics de pression systolique se désynchronisent entre les deux ventricules. Dans cette situation, une élévation de la postcharge gauche présente deux bénéfices: elle augmente la contractilité du VG par effet Anrep, et elle replace le septum dans une position bombée vers la droite par accroissement de la pression intraventriculaire gauche. Rectifier la position du septum diminue également la dilatation de l'anneau tricuspidien et réduit le degré d'insuffisance tricuspidienne [5]. D'où l'efficacité d'une vasoconstriction systémique (élévation des RAS) dans la prise en charge de la défaillance droite.
Le risque d’ischémie myocardique du VD augmente au fur et à mesure que la PAP s’élève. En effet, la perfusion coronarienne du VD est systolo-diastolique, contrairement à celle du VG qui est essentiellement diastolique (Figure 14.13).
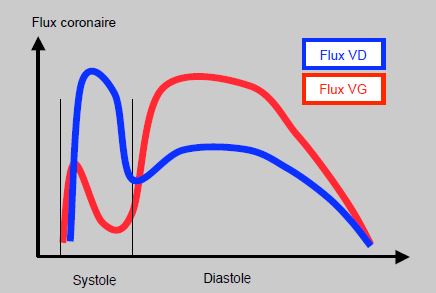
Figure 14.13 : Flux coronarien droit et gauche. Schéma du flux coronarien systolo-diastolique dans le ventricule droit (trait bleu) et dans le ventricule gauche (trait rouge). En systole, la pression normale de l’aorte est bien plus haute que celle du VD, alors qu’elle est la même que celle du VG ; le flux est donc important dans le réseau coronarien qui dessert le VD, mais il est inexistant dans celui du VG, sauf en protosystole pendant le début de la contraction isovolumétrique. La compression systolique des vaisseaux intramyocardiques du VG stoppe le flux coronarien, ce qui n’est pas le cas dans le VD dont la pression systolique est cinq fois plus basse que celle de l’aorte. Si la pression systolique du VD s’élève et se rapproche de celle du VG, la composante systolique de sa perfusion coronaire est progressivement perdue, d’où le risque d’ischémie droite en cas d’hypertension pulmonaire.
Bien que la pression diastolique systémique reste supérieure à la pression diastolique pulmonaire, le rapprochement des deux pressions systoliques en cas d’HTAP sévère diminue la pression de perfusion coronarienne du VD en réduisant sa composante systolique; amputée de presque la moitié de son apport en O2, la perfusion coronarienne droite prédomine en diastole et ressemble alors à celle du VG [2]. La perfusion coronarienne droite est améliorée par une augmentation de la pression systémique par des vasoconstricteurs.
Chez le petit enfant, l’insuffisance ventriculaire congestive se manifeste par des difficultés d’alimentation et un retard de croissance, et, dans les cas sévères, par une apathie et un cri affaibli. On voit aussi apparaître une irritabilité, une tachycardie, des efforts inspiratoires excessifs (rétraction intercostale, mouvement des ailes du nez) et une hépatomégalie [4].
Moyens diagnostiques
L'échocardiographie est l'examen primordial parce que le plus simple et le moins invasif. De plus, les fenêtres transthoraciques offrent des images d'excellente qualité chez l'enfant. L'écho 2D fournit des renseignements sur l’anatomie de base, sur la morphologie et la fonction des chambres cardiaques, sur les valves et leur fonctionnement. Le Doppler mesure les flux, les gradients, les shunts et, de manière indirecte, la pression du VD et de l’AP. La forme relativement simple du VG autorise une évaluation quantitative assez précise de sa fonction au moyen d'approximations géométriques qui permettent d'en calculer la fraction d'éjection (FE). Toutefois, la FE n'est pas un critère satisfaisant de la fonction systolique dans les cardiopathies congénitales à cause des modifications morphologiques majeures des ventricules et de leurs conditions de précharge ou de postcharge très spéciales. Les dimensions systoliques et diastoliques sont de meilleurs éléments d'appréciation. La situation est encore plus difficile pour le VD dont la morphologie complexe et le remodelage important excluent l'utilisation des approximations géométriques applicables au VG. La mesure de l'accélération (dP/dt) de la contraction isovolumétrique et l'évaluation de la déformation locale (strain et strain rate) sont des techniques plus précises et moins dépendantes de la forme du VD et de ses conditions de charge [12,14]. La mesure du déplacement de l'anneau tricuspidien (TAPSE tricuspid annular plane systolic excursion), considérée comme un excellent reflet de la contraction longitudinale du VD chez l'adulte, est mal corrélée à la performance ventriculaire chez l'enfant lorsque la postcharge est anormale comme dans une sténose pulmonaire ou un VD systémique, probablement à cause de la prédominance de la musculature circulaire dans ce contexte [8]. L'écho 3D apporte davantage de précision dans l'évaluation du VD, mais il tend à sous-estimer le volume de ce dernier par rapport à l'IRM [1].
L'IRM permet une reconstruction tridimensionnelle très fine de l’anatomie et surpasse clairement l’écho pour l’évaluation du VD, du volume des cavités, des caractéristiques tissulaires (viabilité) et des vaisseaux extracardiaques (veines pulmonaires, aorte, AP, collatérales). Toutefois, elle demande des périodes d'apnée de 10-20 secondes pour l'acquisition des images, un rythme cardiaque régulier et peu rapide, et une immobilité difficile à obtenir sans sédation profonde ou anesthésie générale chez l'enfant [9]. L'angio-CT multibarrettes offre la meilleure résolution spatiale des structures, notamment extracardiaques (vaisseaux, shunts, coronaires), mais présente l’inconvénient d’utiliser des radiations ionisantes (40-70 mGy) et des produits de contraste; la nouvelle génération à double-source et 128 barrettes diminue l'irradiation et restreint la nécessité d'une apnée [6]. Le CT-scan réclame également une fréquence cardiaque assez basse et une immobilité.
L'IRM et le CT ne sont pas sans risque à cause de l'anesthésie qu'ils impliquent chez le petit enfant. Comme la sédation doit être profonde pour obtenir l'immobilité des petits enfants, le danger d'hypoventilation et d'hypercarbie est excessif chez tous ceux qui souffrent d'hypertension pulmonaire ou sont à risque d'une poussée d'HTP. De ce fait, l'anesthésie générale avec intubation et ventilation contrôlée est en général préférable en dessous de 6 ans: induction au sevoflurane, maintien avec sevoflurane ou propofol (1-2 mg/kg/h), curarisation (rocuronium ou vecuronium). Les périodes d'apnée sont gérées par une simple déconnexion respiratoire, qui peut même se faire depuis le poste de contrôle avec un système en cercle extra-long [13]. En effet, le taux de complication varie de 8% à 28%; il consiste essentiellement en épisodes d'hypotension ou de bradycardie, mais aussi en décompensation ventriculaire et en en arrêt cardiaque. Le jeûne doit être limité et l'hydratation doit être assurée par une perfusion intraveineuse (10-20 mL/kg pour la durée de l'examen) vu les risques d'hypotension et de thrombose de shunt [10,13]. La surveillance post-interventionnelle doit être prolongée jusqu'au lendemain dans 10-25% des cas selon l'état clinique et la pathologie [6].
| Dysfonction ventriculaire |
|
A l’exception de la CIA, de la petite CIV et du canal artériel opérés en bas âge, la fonction ventriculaire des congénitaux ne peut jamais être considérée comme normale. Le manque de réserve, la dysfonction ou la défaillance ventriculaire tiennent à plusieurs phénomènes:
- Remodelage anatomique
- Opération palliative
- VD sous-aortique (systémique), ventricule unique
- Longue durée de vie avant correction
- Surcharge de pression, moins bien tolérée que surcharge de volume
- Cyanose
- Ischémie chronique
La défaillance concerne le plus souvent le VD, à cause d'une surcharge de volume (shunt G-D) ou de pression (HTAP, sténose pulmonaire, VD systémique, ventricule unique). L'augmentation de postcharge du VG (↑ RAS) replace le septum interventriculaire en position d'aide au VD.
L'échocardiographie est l'examen de premier choix pour la fonction ventriculaire. L'IRM est plus performante pour la fonction du VD, pour les vaisseaux extracardiaques et pour l'évaluation du volume des cavités. L'IRM et le CT réclament une sédation profonde ou une AG chez le petit enfant. |
© BETTEX D, BOEGLI Y, CHASSOT PG, Juin 2008, dernière mise à jour Février 2018
Références
- CREAN AM, MAREDIA N, BALLARD G, et al. 3D echo systematically underestimates right ventricular volumes compared to cardiovascular magnetic resonance in adult congenital heart disease patients with moderate or severe right ventricular dilatation. J Cardiovasc Magn Resn 2011; 13:78
- CRYSTAL GJ, PAGEL PS. Right ventricular perfusion. Physiology and clinical implications. Anesthesiology 2018; 128:202-18
- DAVLOUROS PA, NIWA K, WEBB G, GATZOULIS MA. The right ventricle in congenital heart disease. Heart 2006; 92(Suppl 1): i27-i38
- DUPUIS C, KACHANER J, FREEDOM R, PAYOT M, DAVIGNON A. Cardiologie pédiatrique, 2ème édition. Paris: Flammarion, 1991, 115-123
- FRIEDBERG MK, REDINGTON MB. Right versus left ventricular failure. Differences, similarities, and interactions. Circulation 2014; 129:1033-44
- GOTTLIEB EA, ANDROPOULOS D. Anesthesia for the patient with congenital heart disease presenting for noncardiac surgery. Curr Opin Anesthesiol 2013; 26:318-26
- HOPKINS WE. The remarkable right ventricle of patients with Eisenmenger syndrome. Coron Artery Dis 2005; 16:19-25
- KOESTENBERGER M, NAGEL B, RAVEKES W, et al. Tricuspid annular plane systolic excursion and right ventricle ejection fraction in pediatric and adolescent patients with tetralogy of Fallot, patients with atrial septal defect, and age-matched normal subjects. Clin Res Cardiol 2011; 100:67-75
- NTSINJANA HN, HUGHES ML, TAYLOR AM. The role of cardiovascular magnetic resonance in pediatric congenital heart disease. J Cardiovasc Magn Reson 2011; 13:51-70
- ODEGARD KC, VINCENT R, BAIJAL RG, et al. SCAI/CCAS/SPA Expert Consensus Statement for anesthesia and sedation practice: recommendations for patients undergoing diagnostic and therapeutic procedures in the pediatric and congenital cardiac catheterization laboratory. Anesth Analg 2016; 123:1201-9
- PETTERSEN E, HELLE-VALLE T, EDVARDSEN T, et al. Contraction pattern of the systemic right ventricle. J Am Coll cardiol 2007; 49:2450-6
- SHERPTONG RWC, MOLLEMA SA, BLOM NA, et al. Right ventricular peak systolic longitudinal strain is a sensitive marker for right ventricular deterioration in adult patients with tetralogy of Fallot. Int J Cardiovasc Imag 2009; 25:669-76
- STOCKTON E, HUGHES M, BROADHEAD M, et al. A prospective audit of safety issues associated with general anesthesia for pediatric cardiac magnetic resonance imaging. Pediatr Anesth 2012; 22:1087-93
- TOYONO M, HARADA K, TAMURA M, et al. Myocardial acceleration during isovolumic contraction as a new index of right ventricular contractile function and its relation to pulmonary regurgitation in patients after repair of tetralogy of Fallot. J Am Soc Echocardiogr 2004; 17:332-7
14. Anesthésie pour la chirurgie cardiaque pédiatrique
- 14.1 Introduction
- 14.2 Physiopathologie
- 14.3 Stratégies hémodynamiques
- 14.3.1 Classification
- 14.3.2 Shunt G → D et débit pulmonaire élevé
- 14.3.3 Hypertension pulmonaire pédiatrique
- 14.3.4 Shunt droit → gauche et débit pulmonaire abaissé
- 14.3.5 Shunt droit → gauche cyanogène et débit systémique abaissé
- 14.3.6 Shunt cyanogène mixte
- 14.3.7 Cardiopathies sans shunt : obstructions et valvulopathies
- 14.3.8 Options thérapeutiques chez le nouveau-né
- 14.3.9 Pharmacothérapie
- 14.4 Techniques d'anesthésie
- 14.5 La CEC chez l'enfant
- 14.6 Approche par pathologie
- 14.6.1 Introduction
- 14.6.2 Repères anatomiques
- 14.6.3 Retours veineux anormaux
- 14.6.4 Communication interauriculaire (CIA)
- 14.6.5 Canal atrio-ventriculaire (CAV)
- 14.6.6 Maladie d'Ebstein
- 14.6.7 Anomalies des valves auriculo-ventriculaires
- 14.6.8 Communication interventriculaire (CIV)
- 14.6.9 Hypoplasie ventriculaire
- 14.6.10 Tétralogie de Fallot
- 14.6.11 Ventricule droit à double issue
- 14.6.12 Atrésie pulmonaire
- 14.6.13 Anomalies de la voie éjectionnelle gauche
- 14.6.14 Transposition des gros vaisseaux
- 14.6.15 Truncus arteriosus
- 14.6.16 Coarctation de l'aorte
- 14.6.17 Anomalies artérielles
- 14.6.18 Transplantation cardiaque
- 14.7 Conclusions